
Disponible
El último concepto agregado al principio ALCOA + es la disponibilidad de datos.
Este punto es una consecuencia del anterior (Durabilidad del Dato), es decir, los datos no solo deben existir, sino que también deben ser accesibles cuando sea necesario, durante todo el ciclo de vida de los datos.
La disponibilidad garantiza que los datos cumplan su uso, ya que pueden usarse cuando sea necesario y por tanto deben estar accesibles en cualquier momento durante la vida útil requerida. Esto también se aplica a cualquier metadato asociado.
Además, los datos deben estar disponibles, de forma segura, para las personas que los necesitan.
Sin lugar a dudas, la forma más eficiente de lograr el principio de disponibilidad es registrar los datos electrónicamente.
Veamos un ejemplo de una carta de advertencia de la FDA para explicar mejor cómo debe aplicarse el concepto de Disponibilidad a las compañías farmacéuticas:
FDA Warning Letter 320-19-16 (Marzo 2019)
Su empresa no se aseguró de que los registros de laboratorio incluyeran datos completos derivados de todas las pruebas necesarias para garantizar el cumplimiento de las especificaciones y estándares establecidos (21 CFR 211.194 (a)).
No retienen los datos de laboratorio generados por sus analistas. Durante nuestra inspección, su personal le dijo a nuestro investigador que las hojas de trabajo de laboratorio de su empresa solo contienen resultados finales de laboratorio. No retiene registros de pesos de muestra escritos en papel. Los documentos se descartan después de que su personal realiza los cálculos.
Debido a que no retuvo los datos de laboratorio, nuestro investigador no pudo confirmar la validez de sus resultados. No puede proporcionar ninguna justificación por no mantener los datos completos. Su personal además declaró a nuestro investigador que, si una preparación de muestra no es buena, se tira y se reinicia. El personal no retiene esos datos.
SherpaPharma ofrece datos con disponibilidad completa, en un entorno de alta seguridad y trazabilidad.
Se puede acceder al sistema a través de Internet. Cualquier usuario aprobado, con el perfil correcto, puede acceder al sistema desde cualquier ubicación.
Mediante el uso de filtros de fecha y la combinación con cualquier otro criterio de filtrado (por ejemplo, área de fabricación, operadores, condiciones de muestreo, microorganismos identificados, etc.), los usuarios acceden instantáneamente a los datos de muestra necesarios, incluida toda la información relacionada. Por ejemplo, en caso de una OOS o una investigación, los usuarios pueden verificar rápidamente si la incidencia es nueva o si se ha repetido en las mismas condiciones o en condiciones diferentes. Los planes CAPA pueden usar SherpaPharma para confirmar si las acciones son efectivas, con cambios de tenencia desde la aplicación de una medida correctiva.
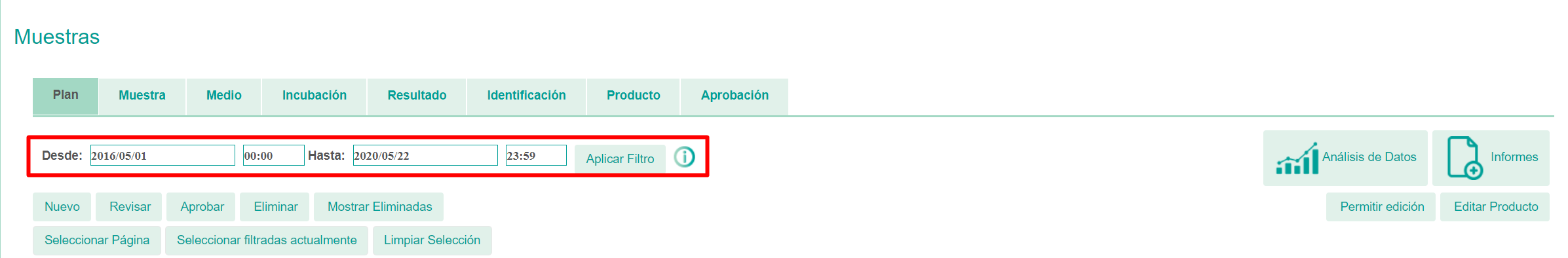
Figura 1. Filtrado de muestras por fecha utilizando SherpaPharma.

Figura 2. Filtrado de actividades en Audit Trail en un periodo de tiempo utilizando SherpaPharma.

Figura 3. Filtrado de las Sesiones de Muestreo en un periodo de tiempo utilizando SherpaPharma.
Además, todos los datos se almacenan de forma segura en una base de datos que se copia diariamente en una ubicación geográfica diferente. El sistema se monitorea continuamente y se actualiza periódicamente para garantizar que los datos estén disponibles siempre y sin ocupar espacio en su ubicación.
Los usuarios de SherpaPharma ya no necesitan un archivo para la documentación microbiológica GMP de muestras ambientales o servidores locales para sus copias de seguridad de datos y metadatos.